Nachrichten
Kontrollierter Giftmord – Studie unter Beteiligung des LOEWE-Zentrums TBG gibt tieferen Einblick in die Regulation bakterieller Wirkstoffe, wichtig auch für die Humanmedizin
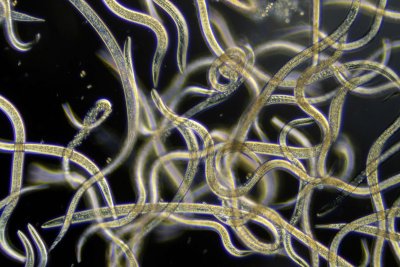
In der Natur leben verschiedene Organismen häufig in Symbiose und profitieren damit voneinander. So auch einige Fadenwürmer, die gemeinsam mit Bakterien aus den Gattungen Photorhabdus und Xenorhabdus ihre Beute „erlegen“. Sobald die Fadenwürmer in ihrer Opfer, vorzugsweise Insektenlarven, eingedrungen sind, übernehmen die Bakterien die Regie und töten die Larve mit giftigen Substanzen. Ein Team von Wissenschaftler:innen aus Frankfurt am Main und Jena identifizierte nun einen Regulator, der die bei diesem Beutezug ablaufenden biologischen Prozesse maßgeblich beeinflusst.Diese sogenannte obligatorische Symbiose, bedeutet das beide Partner – in diesem Fall Fadenwürmer und Bakterien – aneinander gebunden sind und in der Natur nicht ohne den anderen existieren könnten. Denn der Fadenwurm profitiert von Giftbildung seines Bakteriums und das Darmbakterium erhält einen geschützten Lebensraum. Dort produziert es dann eine komplexe Mischung verschiedener Moleküle, sogenannte Sekundärmetabolite (hier mit giftiger Wirkung). Sekundärmetabolite spielen aber auch in der Humanmedizin eine wichtige Rolle. So basieren zum Beispiel viele der klinisch genutzten Antibiotika und Krebsmedikamente auf bakteriellen Sekundärmetaboliten.
Wie die Bildung dieses Sekundärstoff-Cocktails reguliert wird, ist zum Teil bereits erforscht – nicht jedoch, welche Rolle kleinen Ribonukleinsäuren (sRNA) dabei zukommt. Die an der Studie beteiligten Wissenschaftler:innen konnten nun eine entscheidende Beteiligung dieser sRNAs an der Produktion der Sekundärmetabolite nachweisen: Die als „ArcZ“ bezeichnete sRNA beeinflusst etwa 15 Prozent aller Gene der Bakterien. „Die Produktion der Sekundärmetabolite scheint auch in vielen anderen Bakteriengattungen abhängig von ArcZ zu sein“, erklärt Helge Bode, Professor für Molekulare Biotechnologie an der Goethe-Universität Frankfurt und am LOEWE-Zentrum für Translationale Biodiversitätsgenomik (TBG). „Durch die Aufklärung des zugrundeliegenden Mechanismus können wir nun auch in diesen Bakterien gezielt neue Sekundärmetabolite produzieren, die möglicherweise in Zukunft auch klinisch eingesetzt werden können“, ergänzt Nick Neubacher, Doktorand an der Goethe-Universität Frankfurt und Erstautor der Publikation.
Die gemeinsame Publikation wurde online in der Fachzeitschrift „Nature Microbiology“ veröffentlicht.

