Nachrichten
Einblicke in das Recycling menschlicher Zellen: Forscherteam um Roberto Covino FIAS-Fellow und Wissenschaftler bei LOEWE-CMMS gelingt bedeutender Durchbruch im Verständnis der Autophagie
Zellen besitzen eine ausgeklügelte "Recyclingsystem", die Autophagie. Dieser Begriff aus dem Altgriechischen bedeutet "sich selbstverzehrend" und ist ein komplexer Prozess. Alle Zellkomponenten – wie etwa kleine Moleküle, Zucker, einzelne Proteine, Lipide – sind in einer enorm komplexen Choreografie organisiert, die für das korrekte Funktionieren der Zelle und letztlich für die Gesundheit und das Überleben des gesamten Organismus notwendig ist. Manchmal werden Teile dieser Choreographie beschädigt – etwa ein Proteinkomplex oder eine Membran – und die Zelle muss sie beseitigen, bevor sie ihre normale Funktion beeinträchtigen. Oder eine Zelle leidet unter Nährstoffmangel, sodass sie vorhandene Moleküle nutzen und recyclen muss, um sich auf wesentliche Aktivitäten zu konzentrieren. Auch in diesen Situationen wird die Autophagie aktiviert.
Autophagie beruht auf dem Zusammenwirken zahlreicher regulatorischer Proteine, die die Bildung dieser zellulären „Müllabfuhr“ steuern. Sie sammeln den zum Recycling bestimmten Zellinhalt –beispielsweise defekte Proteine – in Bläschen, den Autophagosomen. Eine entscheidende Rolle bei der Bildung dieser Autophagosomen, den Strukturen, die das abzubauende Material einkapseln, spielt das Protein ATG3.
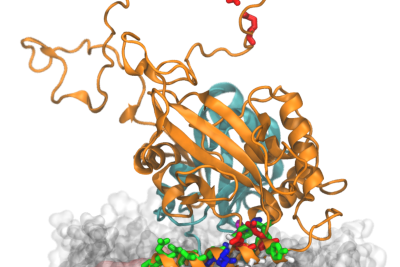
Das Forscherteam um FIAS-Fellow Roberto Covino der auch als Wissenschatler bei LOEWE-CCMS arbeitet, konzentrierte sich bei ihren Untersuchungen auf eine bestimmte Seitenkette des ATG3-Proteins, die amphipathische α-Helix (AHATG3). Sie fanden heraus, dass diese Seitenkette über einzigartige biophysikalische Eigenschaften verfügt: Diese Eigenschaften ermöglichen es ihr, streng kontrolliert mit Membranen zu interagieren. Und sie sind für die Funktion des Proteins bei der Autophagie wesentlich.
Mithilfe modernen Computertechniken, die die Forschenden mit zellbiologischen Experimenten kombinierten, simulierten und beobachteten sie die Dynamik des ATG3-Proteins und seine Interaktion mit Membranen während des Autophagie-Prozesses. Sie fanden heraus, dass die einzigartigen Eigenschaften von ATG3 für einen Schlüsselschritt bei der Autophagosomenbildung entscheidend sind.
Dieses tiefere Verständnis der molekularen Mechanismen, die der Autophagie zugrunde liegen, könnte erhebliche Auswirkungen auf die Entwicklung von Behandlungen für Krankheiten haben, die mit einer gestörten Autophagie einhergehen, wie etwa neurodegenerative Erkrankungen und Krebs.
Publikation:
Taki Nishimura, Gianmarco Lazzeri, Noburu Mizushima, Roberto Covino, Sharon A. Tooze, Unique amphipathic α helix drives membrane insertion and enzymatic activity of ATG3.Sci. Adv.9,eadh1281(2023).DOI:10.1126/sciadv.adh1281
Kontakt:
Dr. Roberto Covino Frankfurt Institute for Advanced Studies (FIAS), Tel.: +49 69 798 47659 covino@fias.uni-frankfurt.de

